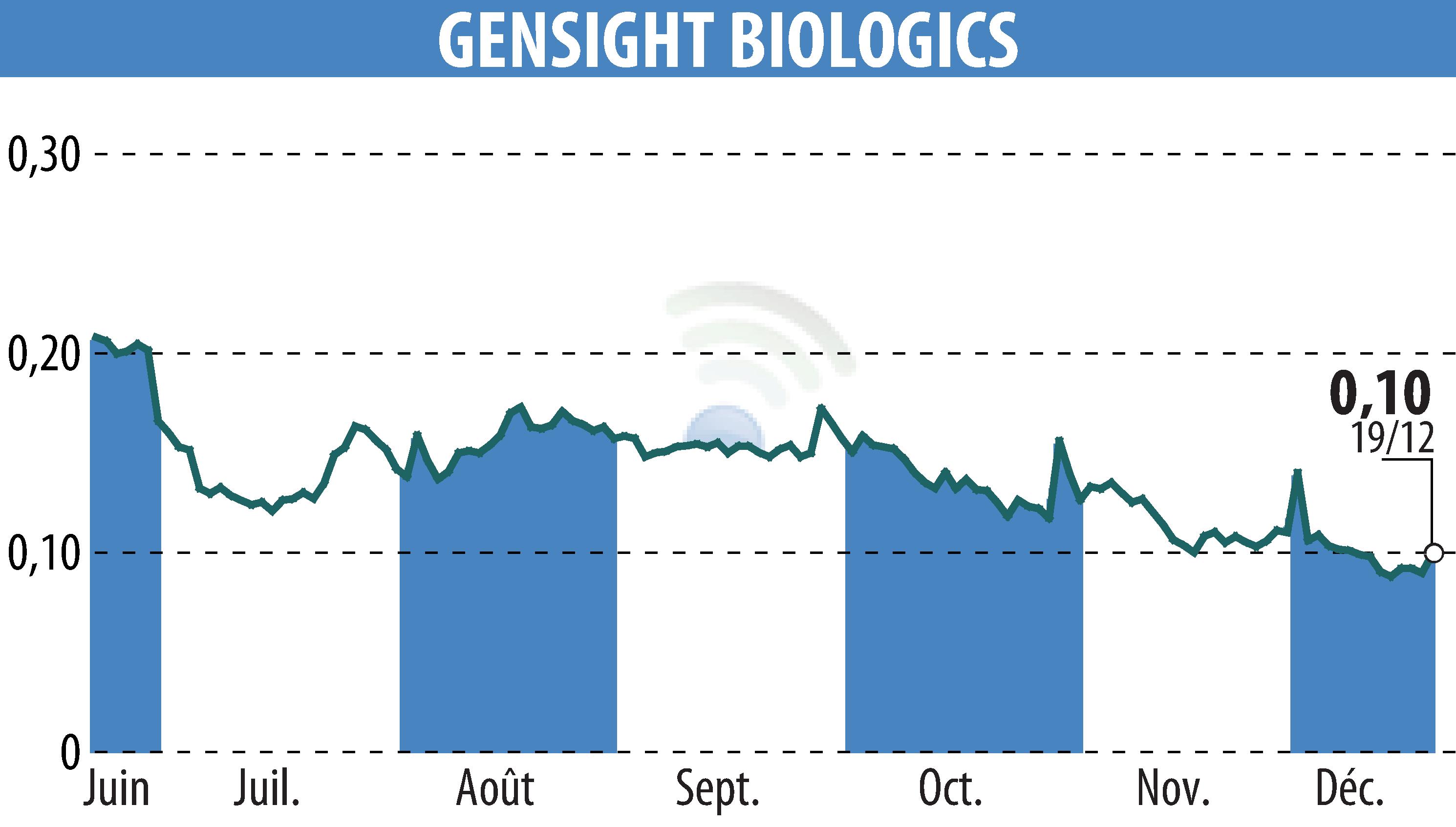
sur GENSIGHT BIOLOGICS S.A. (EPA:SIGHT)
Délivrance d'une autorisation d'accès compassionnel pour GS010/LUMEVOQ®
GenSight Biologics a reçu une autorisation d'accès compassionnel pour sa thérapie génique GS010/LUMEVOQ® de la part de l'Agence nationale de sécurité du médicament et des produits de santé (ANSM). Cette autorisation permet aux patients atteints de Neuropathie Optique Héréditaire de Leber (NOHL) liée à la mutation ND4 de bénéficier du traitement, malgré l'absence d'autorisation de mise sur le marché. Ce dispositif concerne les maladies graves sans alternative thérapeutique.
Les accès compassionnels nécessitent l'initiation de la demande par des professionnels de santé, avec une évaluation préalable par l'ANSM. Les critères d'éligibilité incluent la durée depuis l'apparition de la perte de vision. Cette avancée s'adresse aux cas où le besoin médical n'est pas couvert et repose sur un rapport bénéfice/risque favorable.
R. P.
Copyright © 2025 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de GENSIGHT BIOLOGICS S.A.
