sur GENSIGHT BIOLOGICS S.A. (EPA:SIGHT)
First Steps of the REVISED Clinical Study on GS010/LUMEVOQ®
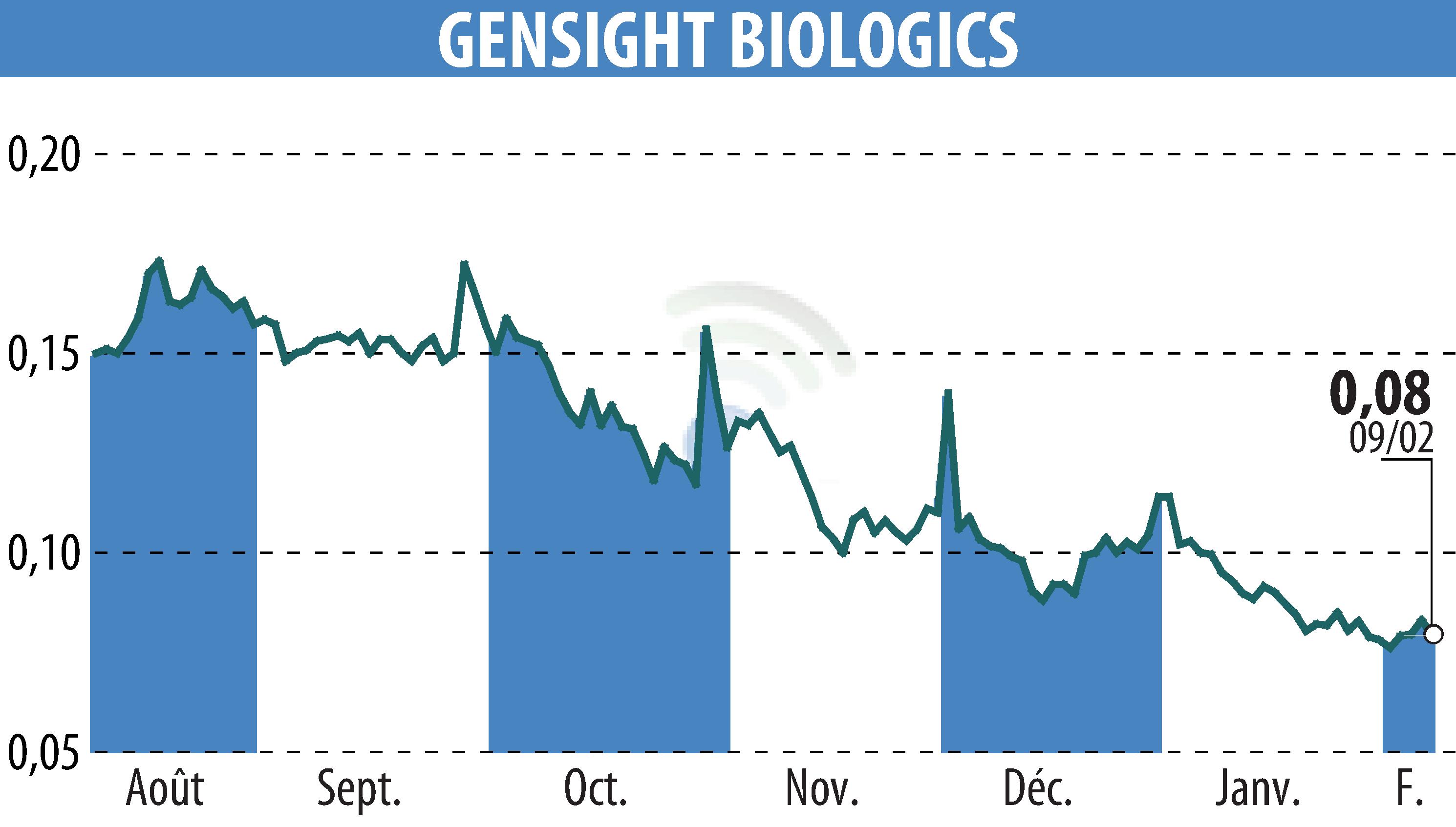
On February 10, 2026, the biopharmaceutical company GenSight Biologics and the Quinze-Vingts National Hospital in Paris announced the treatment of the first patient in the REVISE study. This research, approved in December 2025, is examining the potential of GS010/LUMEVOQ® for Leber hereditary optic neuropathy (LHON), caused by a mutation in the ND4 gene.
The study, conducted exclusively in a hospital setting, will include 14 French patients. The site is also the only one in Europe to administer GS010 under Compassionate Access Authorization. The objective is to evaluate two doses of the gene therapy. Eligible French patients will be given priority for inclusion in the study.
GenSight Biologics plans to launch a new Phase III trial by the end of 2026, highlighting the importance of treating this rare disease. The partnership strengthens their shared mission to advance treatments for rare diseases.
R. P.
Copyright © 2026 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de GENSIGHT BIOLOGICS S.A.
