sur GENSIGHT BIOLOGICS S.A. (EPA:SIGHT)
GenSight Biologics fait le point sur ses programmes d'accès précoce et l'étude REVISE
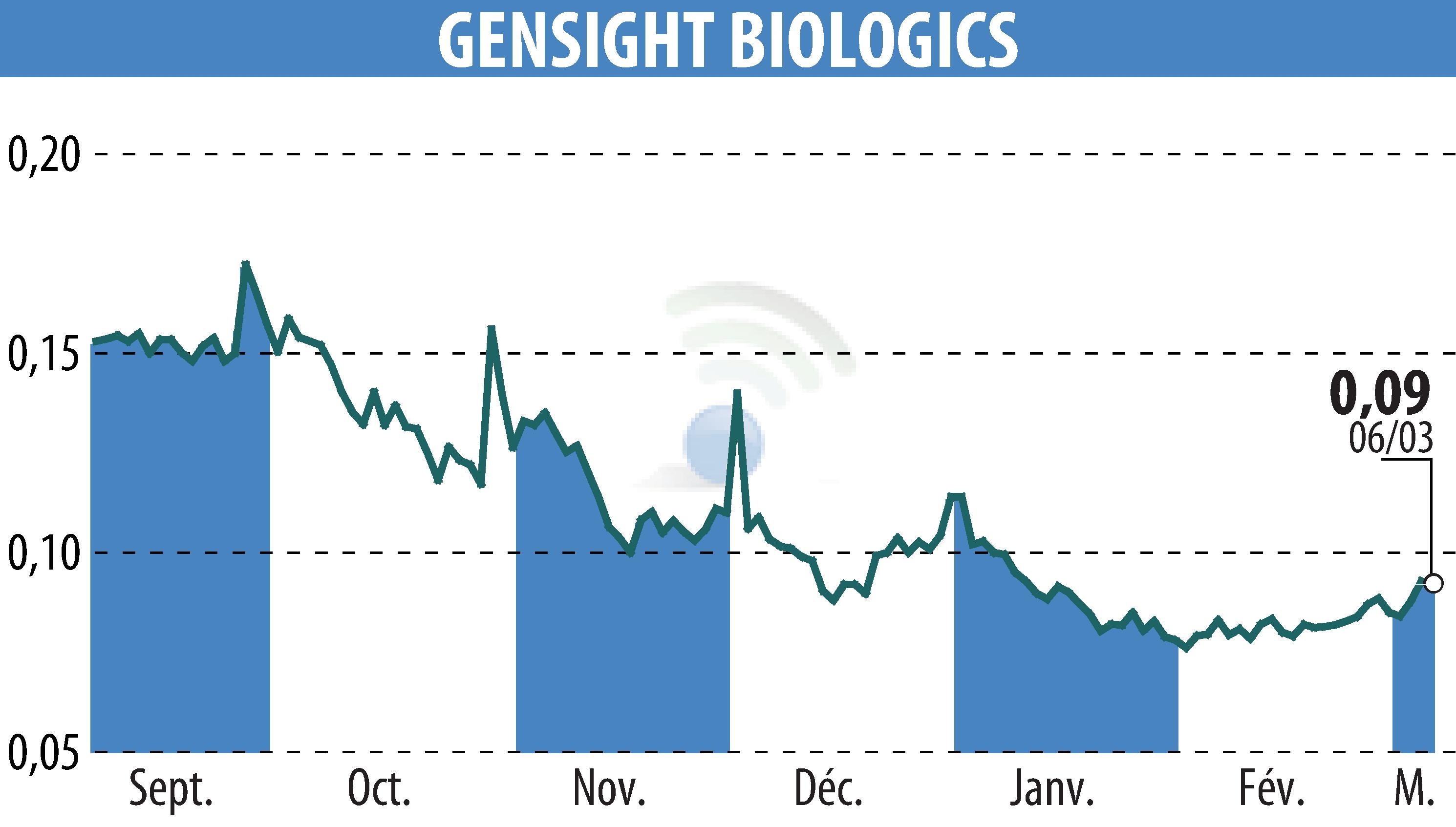
GenSight Biologics a annoncé des progrès dans ses programmes d'accès précoce au GS010/LUMEVOQ® et dans l'étude REVISE en cours. Cette thérapie génique est développée pour traiter la neuropathie optique héréditaire de Leber (LHON), causée par une mutation du gène mitochondrial ND4.
En France, le programme d'accès précoce désigné (AAP) a été approuvé par l'ANSM, permettant le début des traitements à l'Hôpital national dès le mois de mars. L'étude REVISE se déroule comme prévu : le premier patient a été traité en février et un deuxième devrait être inclus prochainement.
En Israël, un deuxième patient a été admis au programme d'accès compassionnel payant. Aux États-Unis, le traitement a également été autorisé pour un deuxième patient dans le cadre du programme d'accès élargi, suite à la récente approbation de la FDA.
Les paiements relatifs aux traitements français sont prévus d'ici fin mars. Ces efforts devraient permettre à l'entreprise de maintenir son financement jusqu'en 2026, soutenant ainsi de futurs projets tels que l'essai de phase III RECOVER.
R. E.
Copyright © 2026 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de GENSIGHT BIOLOGICS S.A.
