sur Heidelberg Pharma AG (ETR:HPHA)
La FDA demande des données supplémentaires à Telix Pharmaceuticals, retardant ainsi le paiement à Heidelberg Pharma
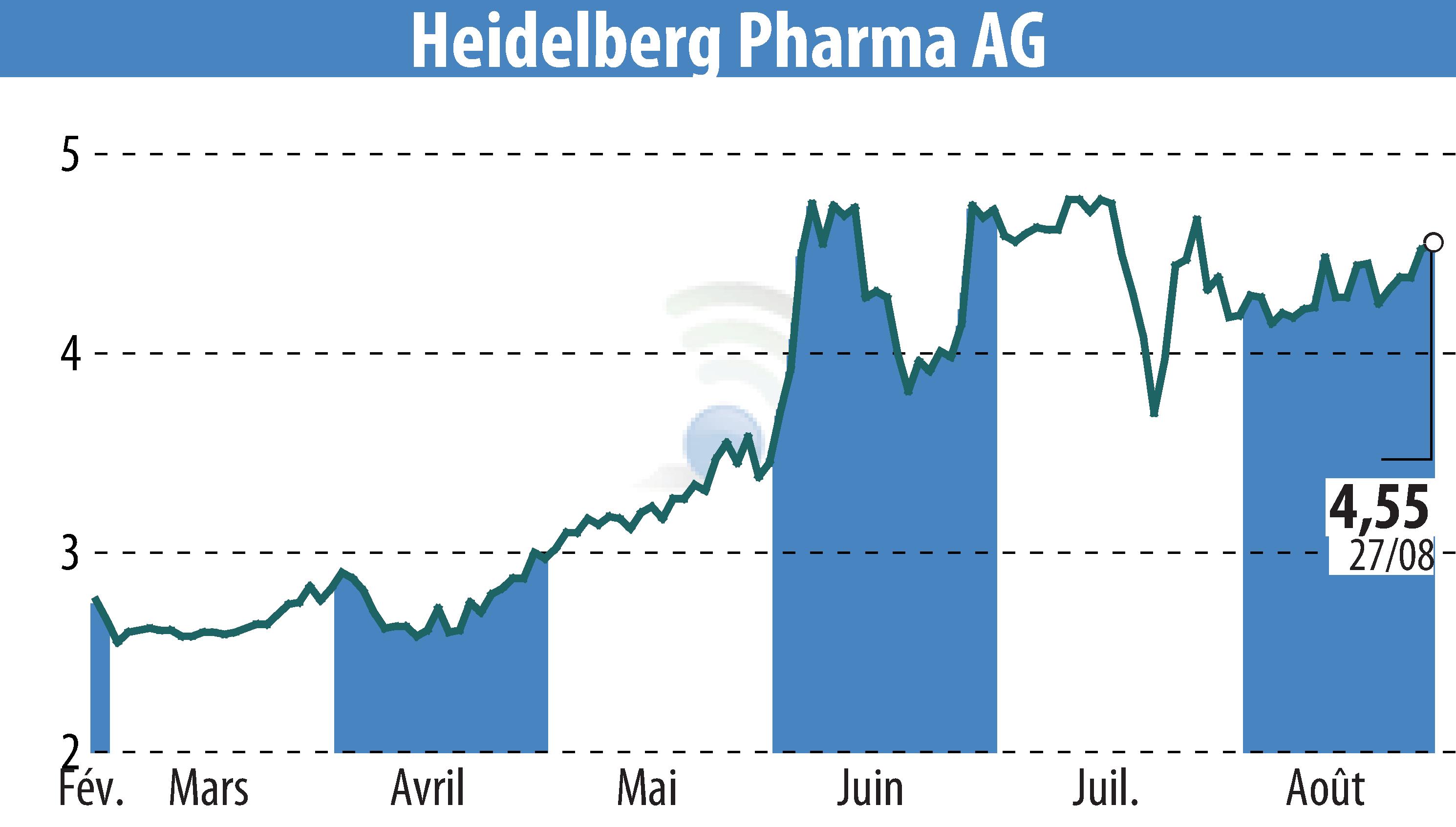
Telix Pharmaceuticals, partenaire de Heidelberg Pharma AG, a rencontré un revers réglementaire concernant son agent d'imagerie, le TLX250-CDx. La FDA a exprimé des inquiétudes concernant le dossier de chimie, de fabrication et de contrôle (CMC), nécessitant des données supplémentaires. Cela a entraîné un retard dans le versement prévu de 70 millions de dollars US par HealthCare Royalty à Heidelberg Pharma.
Telix a soumis une demande d'autorisation de mise sur le marché (BLA) pour le TLX250-CDx, qui a bénéficié d'une évaluation prioritaire. Malgré une acceptation initiale, une lettre de réponse complète a été émise en raison de lacunes identifiées. Telix est chargée de démontrer la comparabilité entre le médicament utilisé dans l'essai de phase 3 ZIRCON et le produit commercial prévu. Deux partenaires tiers doivent également remédier à ces lacunes.
Cette évolution affecte le calendrier financier de Heidelberg Pharma, les réserves de trésorerie devant durer jusqu'au premier trimestre 2026.
R. H.
Copyright © 2026 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de Heidelberg Pharma AG
