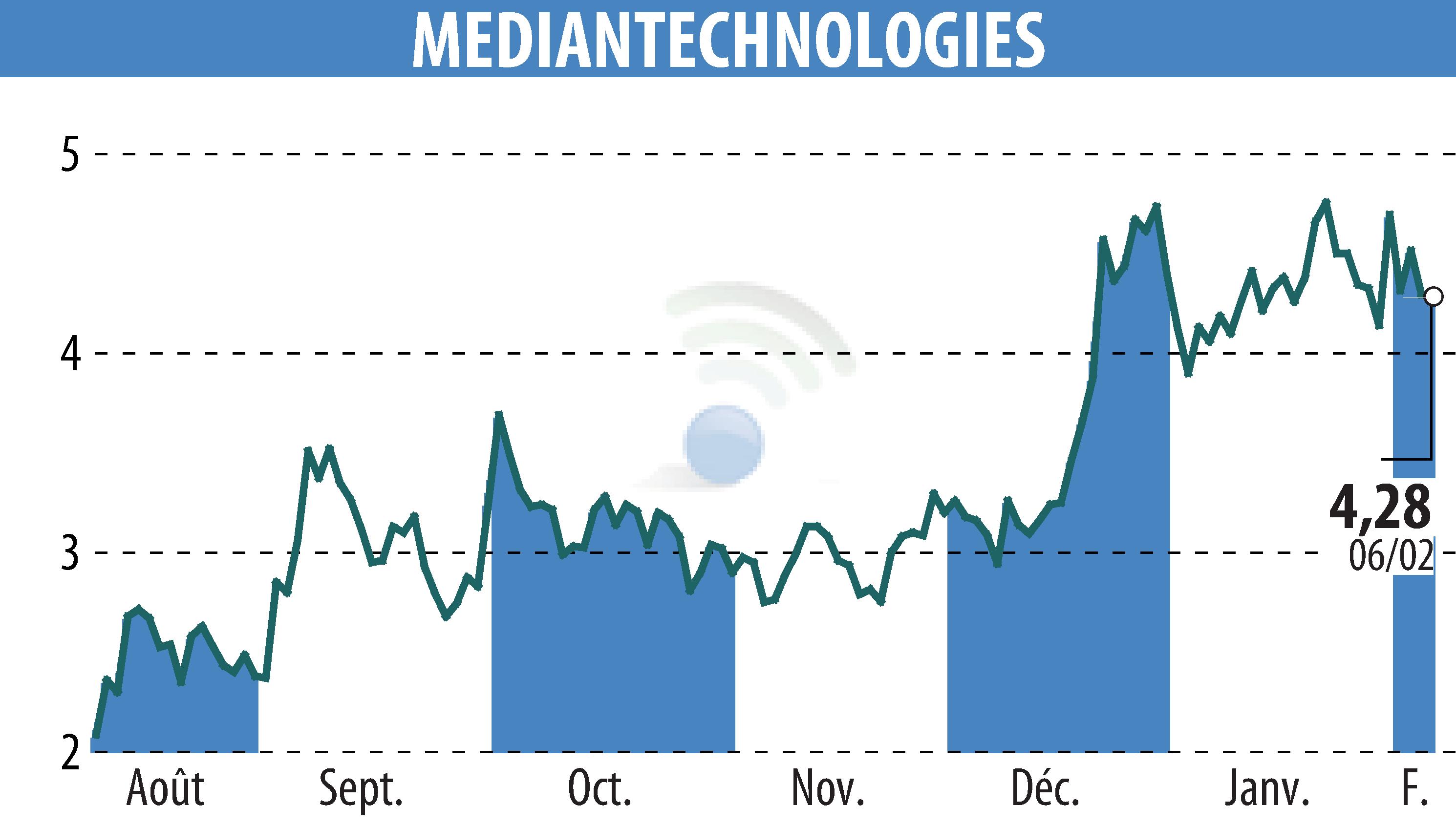
sur MEDIAN TECHNOLOGIES (EPA:ALMDT)
Median Technologies reçoit l'autorisation 510(k) de la FDA pour eyonis® LCS
Median Technologies, basée à Sophia Antipolis, a annoncé que son logiciel d'aide au dépistage du cancer du poumon, eyonis® LCS, a obtenu l'autorisation 510(k) de la FDA. Ce dispositif médical basé sur l'intelligence artificielle vise à offrir un diagnostic précoce, réduisant les faux positifs et limitant les examens inutiles. Avec une sensibilité de 93,3 % et une valeur prédictive négative de 99,9 %, ce logiciel espère transformer le dépistage de quelque 14,5 millions de personnes éligibles aux États-Unis.
Malgré l'accrue des dépistages et la pénurie de radiologues, eyonis® LCS s'intègre aisément dans les systèmes existants, promouvant un suivi plus cohérent et efficace. La société planifie une expansion stratégique aux États-Unis, alliant ventes directes et partenariats de distribution.
Median continue son expansion internationale, visant une certification CE prochainement en Europe. Cette avancée technologique pourrait significativement influencer les diagnostics en oncologie et sauver de nombreuses vies.
R. H.
Copyright © 2026 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de MEDIAN TECHNOLOGIES
