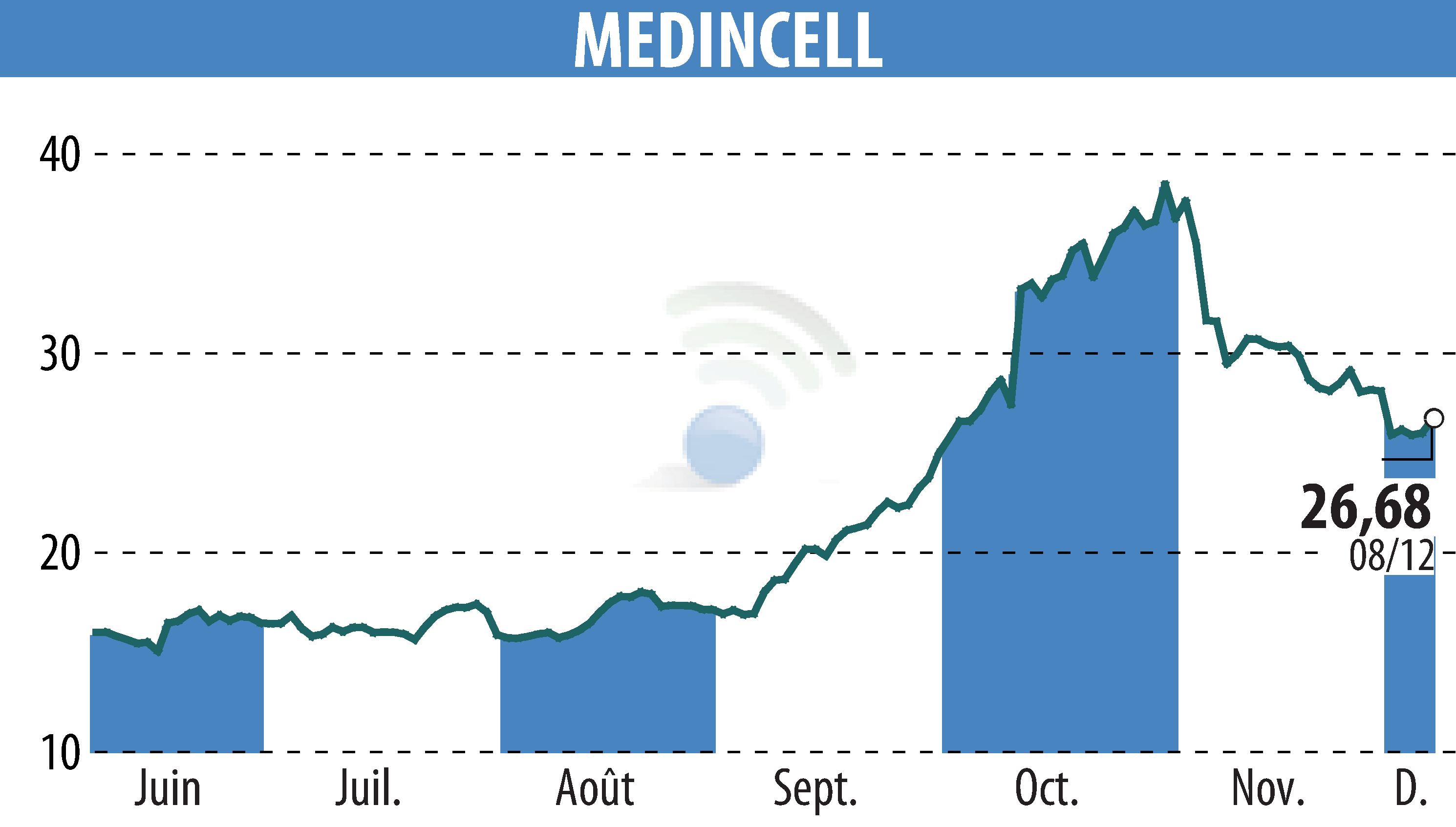
sur MEDINCELL (EPA:MEDCL)
Medincell et Teva soumettent une demande d'autorisation de mise sur le marché auprès de la FDA pour un nouveau traitement injectable.
Teva Pharmaceuticals, en partenariat avec Medincell, a déposé une demande d'autorisation de mise sur le marché auprès de la FDA américaine pour une suspension injectable d'olanzapine à libération prolongée (TEV-749/mdc-TJK). Ce médicament est destiné au traitement de la schizophrénie chez l'adulte, à raison d'une injection mensuelle. Cette formulation injectable d'olanzapine à action prolongée vise à offrir une efficacité comparable à celle de l'olanzapine classique, tout en améliorant l'observance thérapeutique et la stabilité du traitement.
L'examen par la FDA dure généralement deux mois pour l'acceptation et huit mois supplémentaires pour un examen standard. L'olanzapine LAI est conçue pour combler un manque crucial de traitements, en s'attaquant aux problèmes d'observance fréquemment rencontrés dans la prise en charge de la schizophrénie. Le partenariat de Medincell avec Teva s'inscrit dans leur stratégie globale de développement de médicaments injectables à action prolongée pour divers domaines thérapeutiques.
R. P.
Copyright © 2025 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de MEDINCELL
