sur ORPHAN SYNERGY EUROPE-PHARMA (EPA:OSE)
OSE Immunotherapeutics Celebrates FDA Orphan Drug Designation for Pegrizeprument
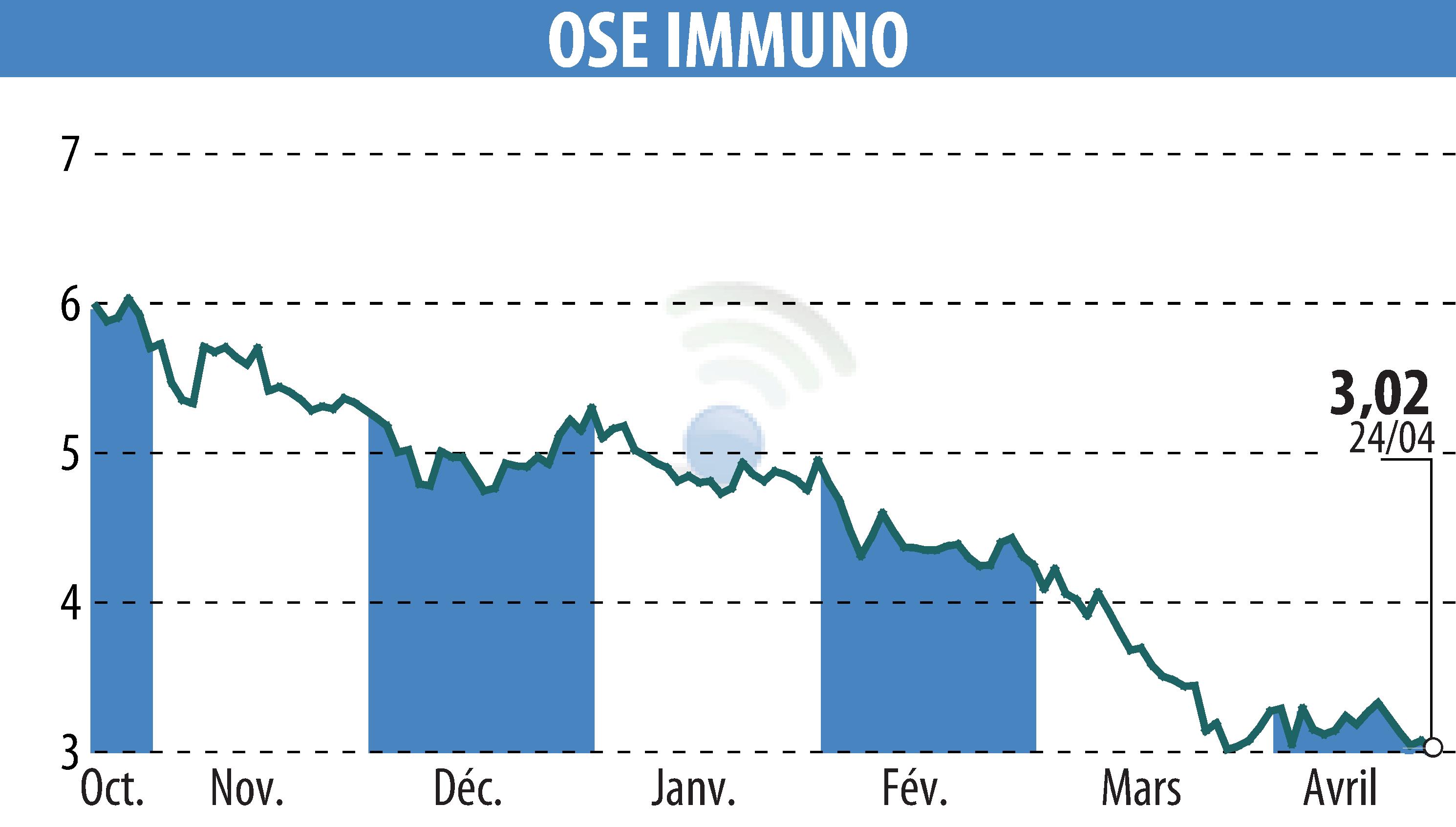
OSE Immunotherapeutics announced that the FDA has granted Orphan Drug Designation to Pegrizeprument (VEL-101) for preventing heart transplant rejection. This declaration follows a previous designation in January 2026 for liver transplant rejection.
Pegrizeprument, an investigational monoclonal antibody fragment, was licensed to Veloxis Pharmaceuticals in 2021. Veloxis handles global development and commercialization.
The FDA’s Orphan Drug Designation targets treatments for rare diseases affecting fewer than 200,000 US patients, aiming to promote drug development for underserved conditions.
Email addresses and contact details are available for investor and media relations, highlighting OSE’s commitment to transparency and engagement with stakeholders.
R. E.
Copyright © 2026 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de ORPHAN SYNERGY EUROPE-PHARMA
