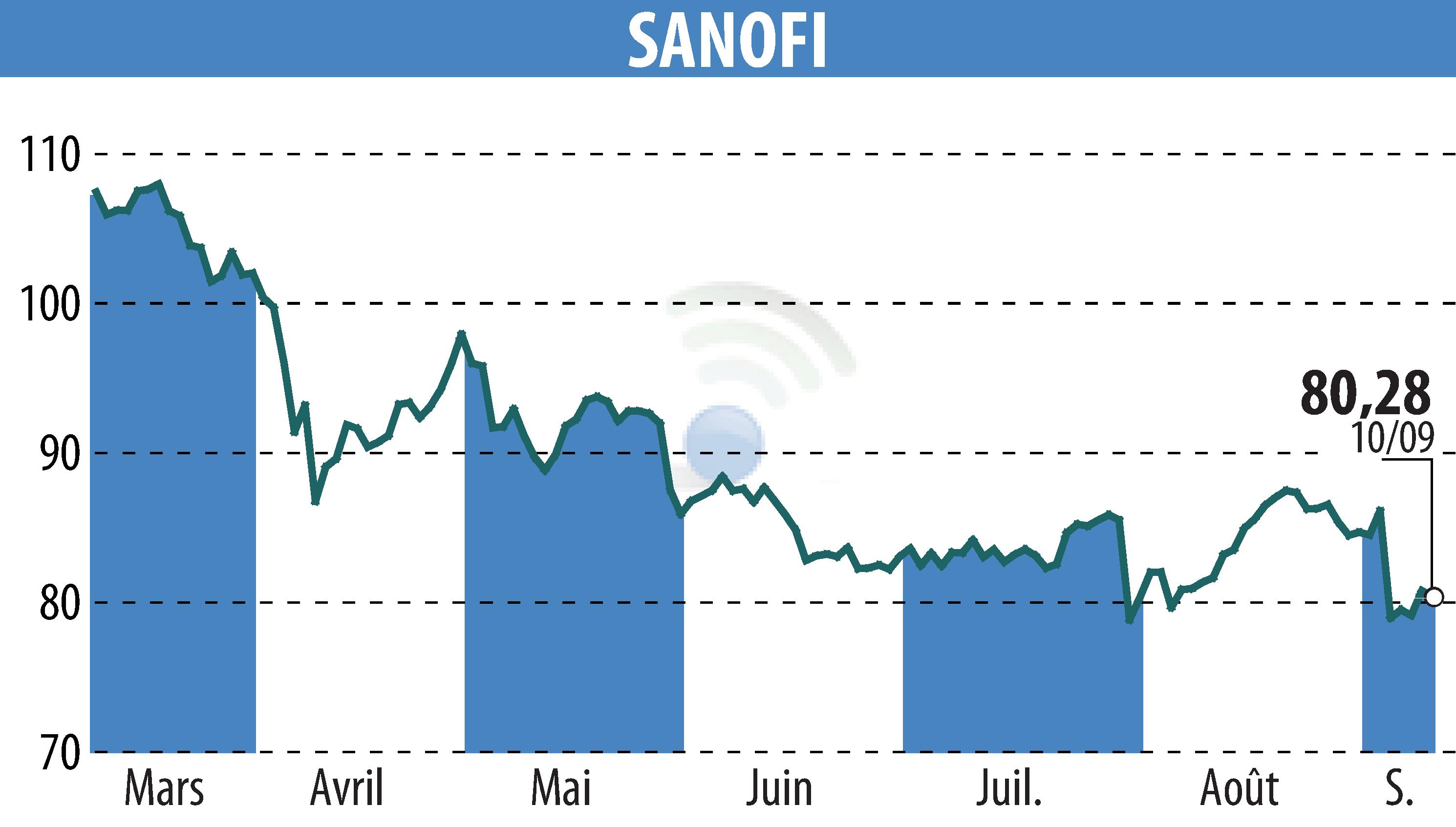
sur SANOFI-AVENTIS (EPA:SAN)
Sanofi obtient une désignation fast track pour le SAR402663 aux États-Unis
Sanofi a annoncé que la Food and Drug Administration (FDA) des États-Unis a accordé la désignation "fast track" à son produit SAR402663. Cette thérapie génique innovante est destinée au traitement de la dégénérescence maculaire liée à l'âge (DMLA) néovasculaire. Cette affection grave peut conduire à une perte de vision importante, impactant plus d'un million d'Américains. La désignation facilitera et accélérera le développement et l'examen de ce médicament, conçu pour inhiber la croissance anormale des vaisseaux sanguins dans l'œil.
Actuellement en phase d'étude clinique I/II, Sanofi évalue l'efficacité du SAR402663 pour réduire les fuites vasculaires et les atteintes rétiniennes. Cette initiative s'inscrit dans les efforts de l'entreprise pour répondre à des besoins médicaux non satisfaits et améliorer la qualité de vie des patients. Avec une administration unique, le traitement pourrait remplacer les injections intravitréennes répétées, simplifiant ainsi la prise en charge des patients.
R. H.
Copyright © 2026 FinanzWire, tous droits de reproduction et de représentation réservés.
Clause de non responsabilité : bien que puisées aux meilleures sources, les informations et analyses diffusées par FinanzWire sont fournies à titre indicatif et ne constituent en aucune manière une incitation à prendre position sur les marchés financiers.
Cliquez ici pour consulter le communiqué de presse ayant servi de base à la rédaction de cette brève
Voir toutes les actualités de SANOFI-AVENTIS
